【化学-物质结构与性质】 (13分)
A、B、C、D、E五种元素,原子序数依次增大,均位于元素周期表前四周期。已知A原子核外有三个未成对电子;A与B形成的一种化合物常温下是红棕色气体;C单质的熔点在同周期单质中最高;D是前四周期中金属性最强的元素;E元素最高价氧化物对应的水化物是一种不溶于水的蓝色固体。请根据以上信息,回答下列问题:
(1)A、B、C三种元素的电负性由小到大的顺序为______(用元素符号表示)。
(2)C的氯化物的熔点比D的氯化物的熔点 (填“高”或“低”),理由是 。
(3)AB2—的VSEPR模型是 ,中心原子的杂化类型是 。
(4)基态D+离子的核外电子排布式是 。
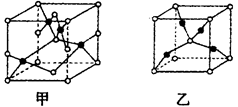
(5)已知B、E能形成晶胞如图所示的两种化合物,化合物的化学式,甲为_______,乙为____________;高温时,甲易转化为乙的原因为__________________。
 H2(g)+CO2(g)△H=
H2(g)+CO2(g)△H=

 -发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
 H++HA-,HA-
H++HA-,HA- 粤公网安备 44130202000953号
粤公网安备 44130202000953号