某校初三化学学习小组的同学前往某地的石灰石矿区进行调查,他们取回矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:
甲组同学:
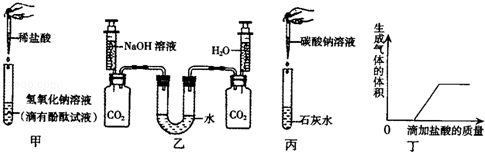
测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与稀盐酸反应,测定反应后生成CO2的体积,再根据体积换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量。下图为大理石与稀盐酸反应的反应装置,并测量CO2的体积。(其他仪器省略)
(1)上图中左侧的橡皮管的作用 。
(2)上图中装置中油层的作用是 。
(3) (填操作方法)可使反应前后油层上方气体压强和外界大气压相同,此时排出水的体积即为生成二氧化碳的体积。
乙组同学:
【查阅资料】1.氢氧化钠溶液可以吸收二氧化碳气体
2.碱石灰可以吸收二氧化碳气体和水分
取样品,研成粉状后,按下图进行实验。
(1)实验步骤:
①连接好装置,检查气密性;
②打开弹簧夹C,在A处缓缓通入一段时间空气;
③称量F的质量;
④关闭弹簧夹C,慢慢滴加稀盐酸至过量,直至D中无气泡冒出;
⑤打开弹簧夹C,再次快速通一段时间空气;
⑥称量F的质量,计算前后两次质量差。最后根据CO2的质量求出样品中碳酸钙的质量
(2)问题探究:
①产品研成粉状的目的 ;
②B装置的作用是 ;
G装置的作用是 。
③若没有E装置,则测定的CaCO3的质量分数会 (填“偏大 偏小 不变”)。
④在步骤②打开弹簧夹C,在A处缓缓通入一段时间空气的目的 。
总结反思:
(1)甲组同学们认为即使排除实验仪器和操作的影响,测定的结果仍不一定准确,甲组中,可能造成实验结果与真实值相比偏小的原因
(2)在乙组实验步骤中,可能造成实验结果与真实值相比偏大的原因 。
 回答下列问题:
回答下列问题: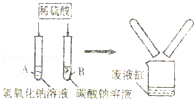
 粤公网安备 44130202000953号
粤公网安备 44130202000953号