近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下: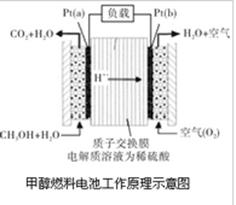
请回答下列问题:
(1)Pt(a)电极对应发生的电极反应为 。Pt(b)电极反生 反应(填“氧化”或“还原”),电极反应为 。
(2)电池的总反应方程式为 。
(3)如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有 mol。
近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:
请回答下列问题:
(1)Pt(a)电极对应发生的电极反应为 。Pt(b)电极反生 反应(填“氧化”或“还原”),电极反应为 。
(2)电池的总反应方程式为 。
(3)如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有 mol。