小华同学为了测定石灰石样品中碳酸钙的质量分数,取相等质量(14.0g)的五份样品分别和稀盐酸反应,其实验数据记录如下表。(杂质既不溶于水也不跟酸反应;不考虑二氧化碳在水中的溶解)通过对数据的分析和比较,回答下列有关问题:
盐酸的质量(g)
|
10
|
20
|
40
|
60
|
80
|
二氧化碳质量(g)
|
0.88
|
1.76
|
3.52
|
4.4
|
X
|
(1)X的数值为。
(2)7.4g氢氧化钙与g碳酸钙含的钙元素质量相等?
(3)请在下图中画出在14.0g样品中加稀盐酸的质量与产生气体质量变化的函数关系示意图。
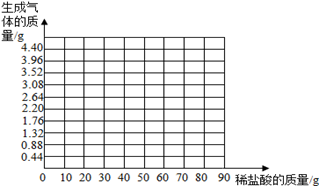
(4)石灰石样品中碳酸钙的质量分数是?(精确到0.1%)