A、B、C、D、E、X六种元素的原子序数依次递增,A、B、C的基态原子中L层未成对电子数分别为3、2、1,D是短周期中原子半径最大的主族元素,E是主族元素且与X同周期,E与C可形成离子化合物,其晶胞结构如图所示。X位于元素周期表中第四周期ⅠB族。请回答下列问题:
(1)D单质晶体中原子的堆积方式为体心立方堆积,其配位数是 。DAB3中阴离子的立体构型是 。中学化学常见微粒中,与晶体D3AB4中阴离子互为等电子体的分子有 (任写一种)。
(2)X2+离子的电子排布式为______,X2+离子与水分子形成的配离子[X(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代有两种不同的结构,试画出[X(H2O)2(Cl)2]具有极性的分子的结构__________。
(3)A元素分别能与硼、铝形成相同类型的晶体,但是A与硼形成晶体的熔点更高,其原因是 。
(4)AC3的沸点比氨的沸点低得多,原因是 。
(5)若E与C形成的晶体的密度为a g·cm-3,则晶胞的体积是_____ cm3 (用NA表示阿伏伽德罗常数的值,写出表达式即可)。
 +、Cl―、Na+、SO42―、Zn2+两两组成的电解质溶液若干种,可选用铜电极、铂电极、锌电极进行电解实验。
+、Cl―、Na+、SO42―、Zn2+两两组成的电解质溶液若干种,可选用铜电极、铂电极、锌电极进行电解实验。 质量不变,应以铂电极为阳极电解___________溶液,或以_________为阳极电解________溶液,前者反应的化学方程式是_________________________。
质量不变,应以铂电极为阳极电解___________溶液,或以_________为阳极电解________溶液,前者反应的化学方程式是_________________________。
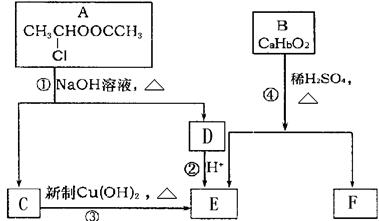
 有A、C两元素的微粒是。(写化学式)
有A、C两元素的微粒是。(写化学式)

 压强/Mpa
压强/Mpa (3)右图是一个电化学装置示意图。用肼——空气燃料电池做此装置的电源。
(3)右图是一个电化学装置示意图。用肼——空气燃料电池做此装置的电源。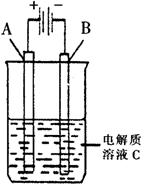
 粤公网安备 44130202000953号
粤公网安备 44130202000953号