下图是实验室利用无水乙醇、冰醋酸和浓硫酸制备乙酸乙酯的实验装置。试回答: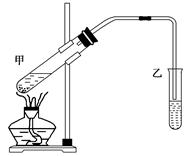
(1)乙酸分子中官能团的名称是__________________。
(2)写出甲中反应的化学方程式_______________________________________________。
(3)小试管乙中饱和Na2CO3溶液的主要作用是__________________________________。
(4)可用____________的方法把制得的乙酸乙酯分离出来。
下图是实验室利用无水乙醇、冰醋酸和浓硫酸制备乙酸乙酯的实验装置。试回答:
(1)乙酸分子中官能团的名称是__________________。
(2)写出甲中反应的化学方程式_______________________________________________。
(3)小试管乙中饱和Na2CO3溶液的主要作用是__________________________________。
(4)可用____________的方法把制得的乙酸乙酯分离出来。