用含少量铁的氧化物的氧化铜制取硫酸铜晶体(CuSO4·xH2O)。有如下操作: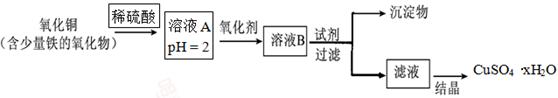
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)溶液A中的金属离子有Fe3+、Fe2+、Cu2+。能检验溶液A中Fe2+的试剂为 (填编号,下同)。
a.KMnO4 b.(NH4)2S c.NaOH d.KSCN
(2)欲用(1)中选择的检验试剂测定溶液A中的Fe2+的浓度,下列滴定方式中(夹持部分略去),最合理的是 (填序号)。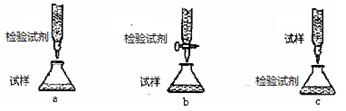
写出滴定反应的离子方程式 。
⑶在上述流程中,要得到较纯的产品,试剂可选用 。
a.NaOH
b.FeO
c.CuO
d.Cu(OH)2
e.Cu2(OH)2CO3
⑷为了测定制得的硫酸铜晶体(CuSO4·xH2O)中 的值,某兴趣小组设计了实验方案:称取mg晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,冷却,称量所得固体的质量为ng。据此计算得
的值,某兴趣小组设计了实验方案:称取mg晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,冷却,称量所得固体的质量为ng。据此计算得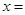 (用含m、n的代数式表示)。
(用含m、n的代数式表示)。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号