已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol 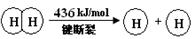
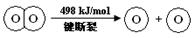
下列说法不正确的是
| A.该反应原理可用于设计氢氧燃料电池 |
| B.破坏1 mol H—O 键需要的能量是463.4 kJ |
| C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol |
| D.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固 |
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol 
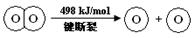
下列说法不正确的是
| A.该反应原理可用于设计氢氧燃料电池 |
| B.破坏1 mol H—O 键需要的能量是463.4 kJ |
| C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol |
| D.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固 |