为了分离甲醇、甲酸、苯、苯酚的混合物,有人设计了下列实验过程。请在括号内填写分离时所用操作方法,并写出方框内有关物质的结构简式。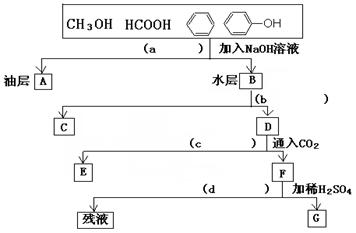
写出下列物质的结构简式A 、C 、
E 、G 。
为了分离甲醇、甲酸、苯、苯酚的混合物,有人设计了下列实验过程。请在括号内填写分离时所用操作方法,并写出方框内有关物质的结构简式。
写出下列物质的结构简式A 、C 、
E 、G 。