A、B、C、X均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去),下列说法错误的是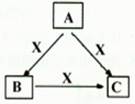
A、若X为Cl2,则C可能为FeCl3
B、若X为KOH溶液,则A可能为AlCl3
C、若X为O2,则A可为硫化氢
D、若A、B、C均为焰色反应呈黄色的物质,则X可能为O2
A、B、C、X均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去),下列说法错误的是
A、若X为Cl2,则C可能为FeCl3
B、若X为KOH溶液,则A可能为AlCl3
C、若X为O2,则A可为硫化氢
D、若A、B、C均为焰色反应呈黄色的物质,则X可能为O2