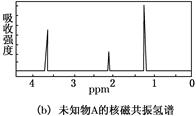
(10分)未知物A的实验式和分子式都是C2H6O。A的红外光谱图如图(a),未知物A的核磁共振氢谱有三个峰图(b),峰面积之比是1∶2∶3。
(1)未知物A的结构简式为________。
(2)未知物A________(“能”或“不能”)萃取碘水中的碘。
(3)在质谱图中,A的最大质荷比是________。
(4)A中________(“有”或“没有”)手性碳原子。
(5)根据“基团理论”, A中的基团名称是________。
(10分)未知物A的实验式和分子式都是C2H6O。A的红外光谱图如图(a),未知物A的核磁共振氢谱有三个峰图(b),峰面积之比是1∶2∶3。

(1)未知物A的结构简式为________。
(2)未知物A________(“能”或“不能”)萃取碘水中的碘。
(3)在质谱图中,A的最大质荷比是________。
(4)A中________(“有”或“没有”)手性碳原子。
(5)根据“基团理论”, A中的基团名称是________。