【化学——选修3:物质结构与性质】
前四周期原子序数依次增大的元素A、B、C、D中,A、B、C均处于第二周期且价电子层中未成对电子数分别为2、3、2:D为ds区元素且最外电子层上只排布了一个电子。
回答下列问题:
(1)D2+的价层电子排布图为 。
(2)A、B、C三种元素中第一电离能由小到大的顺序是 ,电负性最大的是 (填元素符号):
(3)AC32—的立体构型是 ,其中A原子的轨道杂化类型为 ;[D(AB) 4]3—离子中配位数是 。
(4)Y(钇)、Ba(钡)、D、C四种元素组成的一种化合物是高温超导体,其品胞如图所示。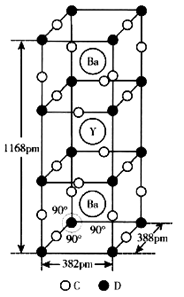
①该化合物的化学式为 ;已知钇、钡的化合价分别为+3、+2,则D2+与D3+的离子数之比为 ;
②列式计算该晶体的密度 g·cm-3。



 分别在三种不同实验条件下进行,它们的起始浓度均为
分别在三种不同实验条件下进行,它们的起始浓度均为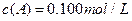 、
、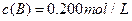 及
及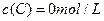 。反映物A的浓度随时间的变化如下图所示。
。反映物A的浓度随时间的变化如下图所示。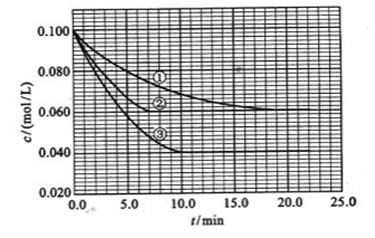

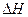 >0,判断其理由是________________;
>0,判断其理由是________________;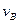 =___________;
=___________;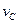 =_______________。
=_______________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号