已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,其中A与B形成可使红色石蕊试纸变蓝的气体,C的最高价氧化物对应水化物呈强碱性,D的离子半径是所在同周期元素简单离子半径中最小的,B与E可形成三角锥型分子且每个原子最外层都满足8电子稳定结构。
(1)B在元素周期表中的位置为第 周期 族,BA3空间构型为 ;
(2)物质甲是C在氧气中燃烧的产物,甲的电子式为 ; C、D、E各自形成的简单离子半径由小到大的顺序为 (用离子符号表示)
(3)E的同族元素的氢化物中沸点最低的是 (写分子式)
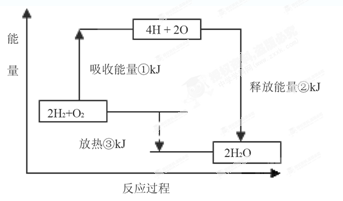
(4)物质乙由A和B元素组成,分子中含18个电子。常温常压下,3.2g液态乙在空气中燃烧生成B的单质,同时放出aKJ热量,该反应的热化学方程式为 。
(5)将10.8g D单质与15.6g甲混合后,完全溶于水中得1L溶液,所得溶液中溶质的物质的量浓度
为 (溶液体积变化忽略不计),产生的气体在标况下体积为 L。

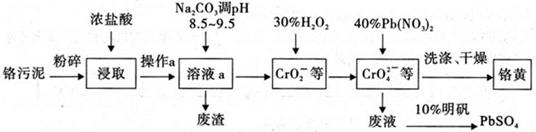
 Al(OH)3+3H+的平衡常数为(保留两位有效数字);
Al(OH)3+3H+的平衡常数为(保留两位有效数字);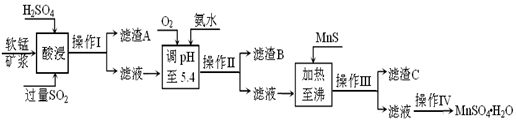

 HAsO42-+OH-,该步水解的平衡常数(25℃)为:(保留两位有效数字)。
HAsO42-+OH-,该步水解的平衡常数(25℃)为:(保留两位有效数字)。 粤公网安备 44130202000953号
粤公网安备 44130202000953号