向甲、乙两恒温恒容的密闭容器中分别充入一定量的A和B,发生反应: A(g)+B(g) xC(g) △H<O。测得两容器中c(A)随时间t的变化如图所示:
xC(g) △H<O。测得两容器中c(A)随时间t的变化如图所示: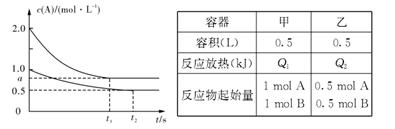
下列说法正确的是
A.x =1
B.Q1<2Q2
C.根据题中信息无法计算a值
D.保持其他条件不变,起始时向乙容器充人0.2 mol A、0.2 mol B、0.2 mol C,则此时v(正) >v(逆)
向甲、乙两恒温恒容的密闭容器中分别充入一定量的A和B,发生反应: A(g)+B(g) xC(g) △H<O。测得两容器中c(A)随时间t的变化如图所示:
xC(g) △H<O。测得两容器中c(A)随时间t的变化如图所示:
下列说法正确的是
A.x =1
B.Q1<2Q2
C.根据题中信息无法计算a值
D.保持其他条件不变,起始时向乙容器充人0.2 mol A、0.2 mol B、0.2 mol C,则此时v(正) >v(逆)