(本题共12分)氰酸(化学式:HOCN)是一种有挥发性和腐蚀性的液体,在水中立刻发生如下反应形成盐X(俗名碳铵):HOCN + 2H2O → X。
23.在上述反应所涉及的各元素中,半径最大的元素原子核外电子共占据_______个轨道。
24.能说明氮元素的非金属性比碳元素强的事实是_________(选填编号)。
A.共用电子对偏向:H-N>H-C B.氧化性:NO2>CO2
C.酸性:HNO3>H2CO3 D.沸点:NH3>CH4
25.据测定,氰酸有两种结构,一种分子内含有叁键,称为正氰酸,另一种分子内不含叁键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。请分别写出正氰酸和异氰酸的结构式:_______________、______________。
26.下面是工业上冶炼Cr时会涉及到的反应:
CrO42-+ S+ H2O → Cr(OH)3↓+ S2O32-+
(1)请将方程式补充完整并配平。
(2)上述反应中,若转移了3mol电子,得到的还原产物是 mol。
27.铁和镍(Ni)位于周期表的同一周期同一族,铁和镍在 周期 族。
28.镍粉在CO中低温加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。150℃时,Ni(CO)4分解为Ni和CO。Ni(CO)4是 晶体,Ni(CO)4易溶于下列 (填序号)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液

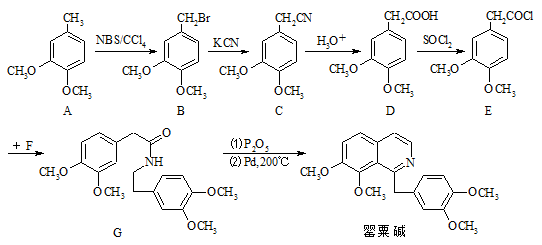
 (R、
(R、 为烃基)。根据已有知识并结合相关信息,写出以乙醇为原料制备
为烃基)。根据已有知识并结合相关信息,写出以乙醇为原料制备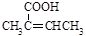 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
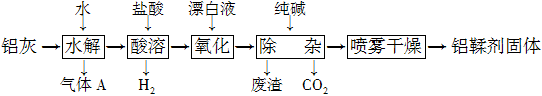
 2 (CN)2↑+12 KCN +N2↑+ Fe3C + C
2 (CN)2↑+12 KCN +N2↑+ Fe3C + C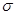 键的数目为 。
键的数目为 。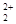 与CN
与CN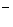 互为等电子体,则O
互为等电子体,则O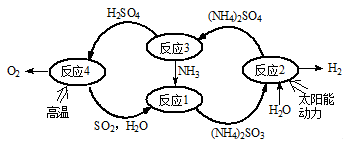
 2SO2(g) + O2(g),△H="+196" kJ•mol-1…………(b)
2SO2(g) + O2(g),△H="+196" kJ•mol-1…………(b)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号