在恒压条件下化学反应:2SO2(g)+O2(g) 2SO3(g);ΔH=-Q kJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是
2SO3(g);ΔH=-Q kJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是
| 容器 |
SO2(mol) |
O2(mol) |
SO3(mol) |
N2(mol) |
Q(kJ) |
| 甲 |
2 |
1 |
0 |
0 |
Q1 |
| 乙 |
1 |
0.5 |
0 |
0 |
Q2 |
| 丙 |
0 |
0 |
2 |
0 |
Q3 |
| 丁 |
1 |
0.5 |
0 |
1 |
Q4 |
A.平衡时,向甲容器中再加1mol O2,一段时间后达到平衡时O2的体积分数减小
B.平衡时,升高丙容器温度,正反应速率增大,逆反应速率减小,平衡逆向移动
C.各容器中反应放出热量的关系为:Q1=2Q2>2Q4
D.丁容器中反应达到平衡时,其化学平衡常数小于乙容器中反应的平衡常数

 溶液中滴加
溶液中滴加 溶液至酸性:
溶液至酸性:
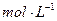
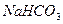 溶液:
溶液: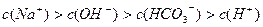
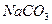 溶液:
溶液: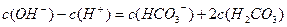
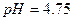 、浓度均为0.1
、浓度均为0.1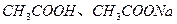 混合溶液:
混合溶液: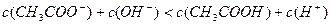

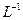 的盐酸滴定0.10 mol•.
的盐酸滴定0.10 mol•.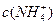 >
>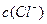 ,
,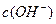 >
>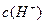
 粤公网安备 44130202000953号
粤公网安备 44130202000953号