如图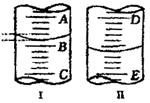
(1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是 mL。
(2)图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号) 。
A.是a mL B.是(25-a)mL
C.一定大于a mL D.一定大于(25-a)mL
(3)写出下列物质的水解离子方程式NaClO溶液: Fe2 (SO4)3 溶液
如图
(1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是 mL。
(2)图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号) 。
A.是a mL B.是(25-a)mL
C.一定大于a mL D.一定大于(25-a)mL
(3)写出下列物质的水解离子方程式NaClO溶液: Fe2 (SO4)3 溶液