工业上用闪锌矿(主要成分为ZnS,还含有CdS、Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:(已知Cd的金属活动性介于Zn和Fe之间)

(1)从滤渣A中可获得一种淡黄色非金属单质的副产品,其化学式为。
(2)浸取时Fe2(SO4)3与ZnS发生反应的化学方程式为。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为。
该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是。
(4)置换法除去重金属离子Cd2+,所用物质C为。
(5)取28.70 g ZnSO4·7H2O加热至不同温度,剩余固体的质量变化如图所示。
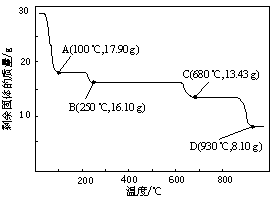
680℃时所得固体的化学式为。
a.ZnO b.Zn3O(SO4)2c.ZnSO4 d.ZnSO4·H2O