盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关。物质A在一定条件下可发生一系列转化,由下图判断下列关系错误的是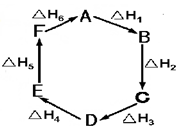
| A.A→F,△H =" -" △H 6 |
| B.△H1+△H 2+△H 3+△H 4+△H 5+△H 6=1 |
| C.C→F,|△H| = |△H 1+△H 2+△H 6 | |
| D.△H 1+△H 2+△H 3 = -△H 4-△H5-△H 6 |
盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关。物质A在一定条件下可发生一系列转化,由下图判断下列关系错误的是
| A.A→F,△H =" -" △H 6 |
| B.△H1+△H 2+△H 3+△H 4+△H 5+△H 6=1 |
| C.C→F,|△H| = |△H 1+△H 2+△H 6 | |
| D.△H 1+△H 2+△H 3 = -△H 4-△H5-△H 6 |