氨的工业合成工艺的成熟推动了人类文明的进步,不少科技工作者为了寻找廉价的氨的制备方法,进行了前赴后继的探索性工作。请回答下列各题:
用氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2+3H2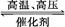 2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
(1)请写出该反应的热化学方程式 。
(2)如果一个反应的ΔH-TΔS<0,则该反应能够自发进行。已知该反应的ΔS="-198.2" J·K-1·mol-1。请判断上述氨气的合成在温度298K时 (能、否)自发发进行。
 下边是日照2
下边是日照2 010年9月11日的空气质量日报
010年9月11日的空气质量日报 (2)写出将A通入下列两种溶液后出现的现象。
(2)写出将A通入下列两种溶液后出现的现象。 能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。 CH3OH(g);下图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H0。(填“>、<或=”下同)
CH3OH(g);下图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H0。(填“>、<或=”下同)

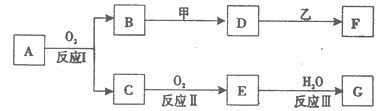
 ;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则: 其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题: 粤公网安备 44130202000953号
粤公网安备 44130202000953号