(14分)人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)蓄电池在放电时起原电池作用,在充电时起电解池的作用。铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应式为 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为_________,当线路中转移0.2mol电子时,则被腐蚀铜的质量为 g
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为___________。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)已知甲醇燃料电池的工作原理如图所示。
该电池工作时,b口通入的物质为___________,该电池正极的电极反应式为:___________,工作一段时间后,当6.4 g甲醇(CH3OH)完全反应生成CO2时,有___________mol电子发生转移。
 CH3OH(g)ΔH1
CH3OH(g)ΔH1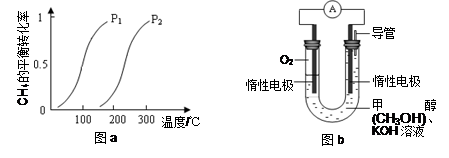
 粤公网安备 44130202000953号
粤公网安备 44130202000953号