煤燃烧的反应热可通过以下两种途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)===CO2(g) ΔH=E1①
b.C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
H2(g)+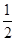 O2(g)===H2O(g)ΔH=E3③
O2(g)===H2O(g)ΔH=E3③
CO(g)+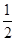 O2(g)===CO2(g)ΔH=E4④
O2(g)===CO2(g)ΔH=E4④
请回答:
(1)与途径a相比,途径b有较多的优点,即______________________________________。
(2)上述四个热化学方程式中的哪个反应ΔH>0?____________。
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是_______。
A.a比b多 B.a比b少 C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为______________________________。
(5)已知:
①CO(g)+1/2O2(g)=CO2(g) ΔH1= -283.0 kJ/mol
②H2(g)+1/2O2(g)=H2O(l) ΔH2= -285.8 kJ/mol
③C2H5OH(l)+ 3O2(g)=2CO2(g)+3H2O(l) ΔH3="-1370" kJ/mol
则④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的ΔH=______________。
 CH3CH2OH(g)+3H2O(g) 25℃时.K=2.95×1011
CH3CH2OH(g)+3H2O(g) 25℃时.K=2.95×1011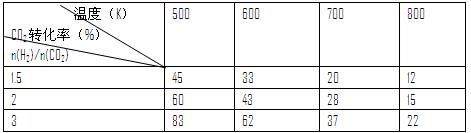
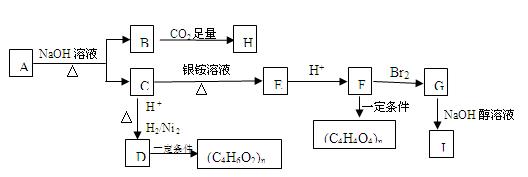

 反应。
反应。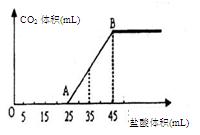


 粤公网安备 44130202000953号
粤公网安备 44130202000953号