根据所给信息填空
已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。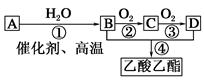
回答下列问题:
(1)A、B、C、D中所有原子都在同一平面上的是________。
(2)写出下列反应的反应类型:①________,④________。
(3) B、D的结构简式 ,
根据所给信息填空
已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
回答下列问题:
(1)A、B、C、D中所有原子都在同一平面上的是________。
(2)写出下列反应的反应类型:①________,④________。
(3) B、D的结构简式 ,