硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2。850℃~950℃时,硫铁矿在空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4∶1):
3FeS2 + 8O2 = Fe3O4 + 6SO2 ①
4FeS2 + 11O2 = 2Fe2O3 + 8SO2 ②
(1)含硫35%的硫铁矿样品(杂质不含硫),其FeS2的含量为_________________。
(2)设1 t纯净的FeS2按②式完全反应,产生标准状况下SO2__________ m3。
(3)为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,所得炉气中SO2的体积分数为多少? 。
(4)480 g纯净的FeS2在空气中完全反应,若所得固体中,Fe和O
的物质的量之比n(Fe)∶n(O) =4∶a,此时消耗空气为bmol。
①试写出b与a的关系式:___________________。
②并作出b与a的关系曲线。
 醛是一种重要的化工产品,可利用甲醇催化脱氢制备。气态甲醛与气态甲醇转化的能量关系如图所示。
醛是一种重要的化工产品,可利用甲醇催化脱氢制备。气态甲醛与气态甲醇转化的能量关系如图所示。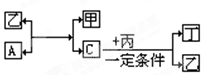
 元素化合价判断丙、丁是否在一定条件下生成单质D,简述判断理由。
元素化合价判断丙、丁是否在一定条件下生成单质D,简述判断理由。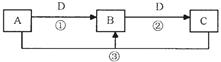
 自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则B的化学式可能是;实验室制取A的离子方程式为。
自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则B的化学式可能是;实验室制取A的离子方程式为。 试剂名称)。
试剂名称)。

 电弧法合成的碳纳米管常伴有大量的杂质—碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其中
电弧法合成的碳纳米管常伴有大量的杂质—碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其中 反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七种。
反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七种。 出来的性质是(填选项序号)__________。
出来的性质是(填选项序号)__________。 粤公网安备 44130202000953号
粤公网安备 44130202000953号