随着能源与环境问题越来越被人们关注,碳一化学成为研究的热点。“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺。
Ⅰ、热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ/mol,在温度和容积相同的A、B、C三个容器中(容器的体积为2L),按不同方式投入反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表:
CH3OH(g)+H2O(g) △H=-49.0kJ/mol,在温度和容积相同的A、B、C三个容器中(容器的体积为2L),按不同方式投入反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表:
| 容器 |
A |
B |
C |
| 反应物投入量 |
1molCO2(g)和 3molH2(g) |
1molCH3OH(g)和 1molH2O(g) |
2molCO2(g)和 6mol H2(g) |
| CH3OH(g)浓度(mol/L) |
c1 |
c2 |
c3 |
| 反应能量变化 |
放出29.4 kJ |
吸收a kJ |
放出b kJ |
①从反应开始到达平衡时,A中用CO2来表示的平均反应速率为 mol/(L· s)(用具体数值表示);
②a= 。c1 c2 1/2c3(填“>”“<”或“=”)。
Ⅱ、CO可用于合成甲醇。在压强0.1MPa条件下,向体积为bL的密闭容器中充入amolCO和2amolH2,在催化剂作用下合成甲醇:CO(g)+2H2(g) CH3OH(g).平衡时CO的转化率与温度、压强的关系如图所示:
CH3OH(g).平衡时CO的转化率与温度、压强的关系如图所示: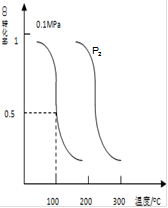
(1)该反应属于反应 (填“吸热”或“放热”);P2 0.1MPa(填“>”“<”或“=”);
(2)100℃时,该反应的平衡常数K= (用含a、b的代数式表示)。
Ⅲ、碳一化合物在治理汽车尾气方面也大有可为,如CO、CH4等在一定条件下均可以与氮氧化物生成无污染的物质。CO与NO在催化剂的条件下反应如下:2NO(g)+2CO(g)⇌2CO2(g)+N2(g) △H<0,在绝热、恒容的密闭容器中加入一定量的NO和CO发生上述反应,下列示意图不能说明反应在进行到t1时刻达到平衡状态的是 (填字母序号)。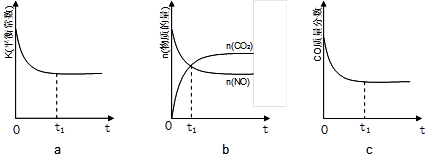
 粤公网安备 44130202000953号
粤公网安备 44130202000953号