甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)  CH3OH(g)下表为不同温度下的平衡常数(K)
CH3OH(g)下表为不同温度下的平衡常数(K)
| 温度 |
250℃ |
300℃ |
350℃ |
| K |
2.041 |
0.270 |
0.012 |
(1)该反应的平衡常数表达式K= ,ΔH 0(填“>”、“<”或“=”)。
(2)将1 mol的H2和 1 mol 的 CO充入 1 L 恒容密闭反应器中,达到平衡后,容器内的压强为开始时的60%,求CO的平衡转化率(写出计算过程)。
(3)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是
(填字母)。
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡时c(H2)/ c(CH3OH)减小
(4)其他条件相同时,在上述三个温度下分别发生该反应。300℃时,H2的转化率随时间的变化如图所示,请补充完成350℃时H2的转化率随时间的变化示意图。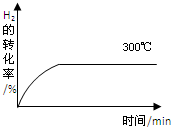
相关知识点
 H2
H2 H2、
H2、 C
C Li
Li Na
Na N
N Li
Li Mg。
Mg。 He的中子数是
He的中子数是  He与
He与 He互称为 。
He互称为 。 He
He He两种核素中,原子核内的中子数相差为 ,与α粒子有相同质子数和中子数的是 。
He两种核素中,原子核内的中子数相差为 ,与α粒子有相同质子数和中子数的是 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号