实验室常用浓盐酸与二氧化锰反应制取少量氯气,反应的化学方程式为:
4HCl(浓) +MnO2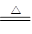 MnCl2+2H2O+Cl2↑,取足量12 mol·L-1浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为4.48L。计算(写出具体计算过程)
MnCl2+2H2O+Cl2↑,取足量12 mol·L-1浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为4.48L。计算(写出具体计算过程)
(1)被氧化的HCl的物质的量 (2) 参加反应的MnO2的质量
实验室常用浓盐酸与二氧化锰反应制取少量氯气,反应的化学方程式为:
4HCl(浓) +MnO2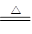 MnCl2+2H2O+Cl2↑,取足量12 mol·L-1浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为4.48L。计算(写出具体计算过程)
MnCl2+2H2O+Cl2↑,取足量12 mol·L-1浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为4.48L。计算(写出具体计算过程)
(1)被氧化的HCl的物质的量 (2) 参加反应的MnO2的质量