Ⅰ.苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是C8H10(g)  C8H8(g)+H2(g)ΔH=120 kJ·mol-1。某温度下,将0.40 mol苯乙烷,充入2 L真空密闭容器中发生反应,
C8H8(g)+H2(g)ΔH=120 kJ·mol-1。某温度下,将0.40 mol苯乙烷,充入2 L真空密闭容器中发生反应,
测定不同时间该容器内气体物质的量,得到数据如下表:
| 时间/min |
0 |
10 |
20 |
30 |
40 |
| n(C8H10)/mol |
0.40 |
0.30 |
0.24 |
n2 |
n3 |
| n(C8H8)/mol |
0.00 |
0.10 |
n1 |
0.20 |
0.20 |
(1)当反应进行到20 min时,该段时间内H2的平均反应速率是_____ ___。
(2)该温度下,该反应的化学平衡常数是________ ________。
(3)若保持其他条件不变,用0.50 mol H2(g)和0.50 mol C8H8(g)合成C8H10(g),当有30 kJ热量放出时,该反应中H2的转化率是________________。此时,该合成反应是否达到了平衡状态?________(填“是”或“否”),且正反应速率 逆反应速率(填大于、小于或等于)
(4)对于反应C8H10(g)  C8H8(g)+H2(g),下列说法正确的是
C8H8(g)+H2(g),下列说法正确的是
A、恒温恒容条件下C8H10(g)和C8H8(g)生成速率相等能说明该反应达到平衡状态
B、压强增大该反应的平衡常数也增大
C、在恒温恒压条件下,有2 mol C8H10(g)在容器中完全反应,该反应的反应热为ΔH1,另有4 mol C8H10(g)在容器中完全反应,该反应的反应热为ΔH2,则ΔH2=2ΔH1
Ⅱ.在一容积为2 L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)  2NH3(g) ΔH<0,反应中NH3的物质的量浓度的变化情况如下图:
2NH3(g) ΔH<0,反应中NH3的物质的量浓度的变化情况如下图: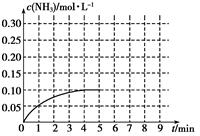
(1)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为________。
①0.20 mol·L-1 ②0.12 mol·L-1 ③0.10 mol·L-1 ④0.08 mol·L-1
(2)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1),请在上图中画出第5分钟末达到此平衡时NH3浓度的变化曲线。
 3
3
 CH3COOH+Na2CO3===2CH3COONa+CO2↑+H2O若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请判断下列反应不能成立的是_______________________(填编号)。
CH3COOH+Na2CO3===2CH3COONa+CO2↑+H2O若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请判断下列反应不能成立的是_______________________(填编号)。 NaHCO3+C6H5OH
NaHCO3+C6H5OH 2SO4⑥HClO4
2SO4⑥HClO4 aCl晶体根据上述反应,总结出复分解反应发生的另一规律:___________________________________________;
aCl晶体根据上述反应,总结出复分解反应发生的另一规律:___________________________________________;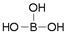 。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面 元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有_______个。
元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有_______个。 粤公网安备 44130202000953号
粤公网安备 44130202000953号