煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.已知:CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ |
400 |
500 |
800 |
| 平衡常数K |
9.94 |
9 |
1 |
试回答下列问题:
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D、E);
| |
n(CO) |
n(H2O) |
n(H2) |
n(CO2) |
| A |
1 |
5 |
2 |
3 |
| B |
2 |
2 |
1 |
1 |
| C |
2 |
1 |
2 |
3 |
| D |
0.5 |
2 |
1 |
1 |
| E |
3 |
1 |
2 |
1 |
(2)在1L密闭容器中通入10 molCO和10 mol水蒸气,在500℃下经过30s达到平衡,则30s内CO的平均反应速率为
(3)已知在一定温度下,C(s)+CO2(g) 2CO(g)平衡常数K;K的表达式 ;C(s)+H2O(g)
2CO(g)平衡常数K;K的表达式 ;C(s)+H2O(g) CO(g)+ H2(g)平衡常数K1; CO(g)+H2O(g)
CO(g)+ H2(g)平衡常数K1; CO(g)+H2O(g) H2(g)+ CO2(g)平衡常数K2;则K、K1、K2之间的关系是:
H2(g)+ CO2(g)平衡常数K2;则K、K1、K2之间的关系是:
(4)某温度、容积固定容器中,投入一定反应物,对可逆反应C(s)+ CO2(g) 2CO(g)不能判断该反应达到化学平衡状态的是
2CO(g)不能判断该反应达到化学平衡状态的是
A.c(CO2)= c(CO)
B.混合气体相对分子质量不变
C.容器中的压强不变
D.v正(CO)= 2v正(CO2)
E.c(CO)保持不变
(5)如图1所示,在甲、乙两容器中都充入1mol C和1mol CO2,并使甲、乙两容器初始容积相等.在相同温度下发生反应C(s)+CO2(g)  2CO(g),并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象.
2CO(g),并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象.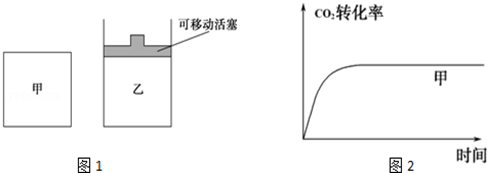

 。
。 2CrO42-+2H+,请写出该平衡的平衡常数表达式k=,若继续加水稀释,平衡将移动(填“正向”、“逆向”“不”)。
2CrO42-+2H+,请写出该平衡的平衡常数表达式k=,若继续加水稀释,平衡将移动(填“正向”、“逆向”“不”)。
 ,反应中若形成
,反应中若形成 键放热103.9k!。则该反应的
键放热103.9k!。则该反应的 =_______。
=_______。
 (高分子化合物),则
(高分子化合物),则 有多种同分异构体,如
有多种同分异构体,如 等。写出其中满足下列条件的同分异构体:
等。写出其中满足下列条件的同分异构体:

 粤公网安备 44130202000953号
粤公网安备 44130202000953号