Na2SO4溶液的溶解度曲线如图,下列说法一定正确的是( )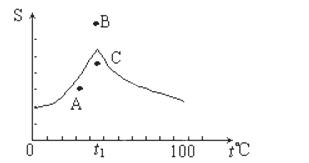
A.A点表示Na2SO4溶液尚未达到饱和,但降温和加入Na2SO4·H2O晶体都可使其饱和
B.B、C点表示t1℃时,Na2SO4溶液在B点的溶解度大于在C点的溶解度
C.在C点时Na2SO4溶液降温或升温,都会使其溶液变澄清
D.制取芒硝的最佳方法是在100℃时配成饱和溶液,再降温至0℃析出晶体
Na2SO4溶液的溶解度曲线如图,下列说法一定正确的是( )
A.A点表示Na2SO4溶液尚未达到饱和,但降温和加入Na2SO4·H2O晶体都可使其饱和
B.B、C点表示t1℃时,Na2SO4溶液在B点的溶解度大于在C点的溶解度
C.在C点时Na2SO4溶液降温或升温,都会使其溶液变澄清
D.制取芒硝的最佳方法是在100℃时配成饱和溶液,再降温至0℃析出晶体