(12分)A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下图为相关实验步骤和实验现象: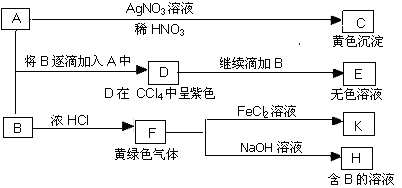
请回答:(1)写出A、B和C的化学式:A ,B ,C 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式: , 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式: 。
(12分)A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下图为相关实验步骤和实验现象:
请回答:(1)写出A、B和C的化学式:A ,B ,C 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式: , 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式: 。