Ⅰ、某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示:
实验步骤:①先连接好装置,检验气密性,加入试剂;②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为 。
(2)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是 。
(3)若将B中品红溶液换成溴水,通入一段时间后溴水褪色,这说明了二氧化硫具有漂白性,你是否同意这个观点 ,(填“同意”或“不同意”),说明理由 (用离子方程式表示)。
Ⅱ、以浓硫酸、浓硝酸、粗铜、水和空气为原料可制得硫酸铜晶体。其过程如下图所示。
回答下列问题:
(4)配平在滤液(Ⅲ)中发生反应的化学方程式:
NOx+ H2O+ O2= HNO3
(5)写出制取硫酸铜的总反应方程式: 。
(6)在上述生产过程中,被循环使用的物质是 。
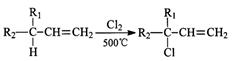
 G、H及丙二酸(HOOCCH2COOH)间转化反应的关系图。A是一种链状羧酸,分子式为C3H4O2;F中含有由七个原子构成的环;H是一种高分子化合物。请填写下列空白:
G、H及丙二酸(HOOCCH2COOH)间转化反应的关系图。A是一种链状羧酸,分子式为C3H4O2;F中含有由七个原子构成的环;H是一种高分子化合物。请填写下列空白:
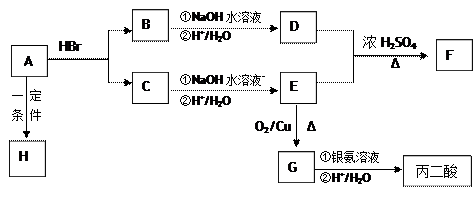
 ,反应类型。
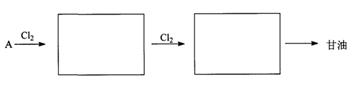
,反应类型。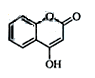 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: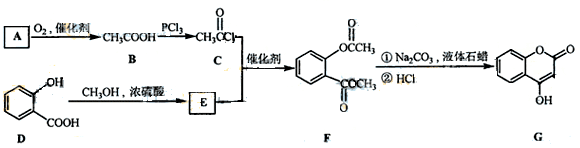 (1)A与银氨溶液反应有银镜生成,则A的结构简式是。
(1)A与银氨溶液反应有银镜生成,则A的结构简式是。
 、
、
 别乙的方法:____________________________________。
别乙的方法:____________________________________。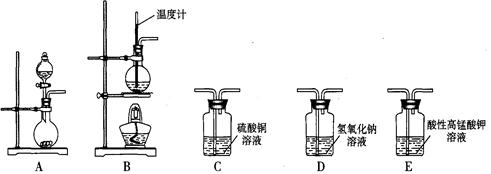
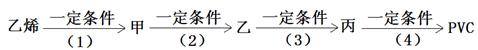
 粤公网安备 44130202000953号
粤公网安备 44130202000953号