已知有些晶体按比例含有一定量特殊的水(称为结晶水),在一定的温度下可脱去结晶水,为了研究草酸亚铁晶体的组成,称取54.0g草酸亚铁晶体在隔绝空气条件下加热,得到剩余固体的质量随温度变化曲线如图所示.已知:温度
时,草酸亚铁晶体完全脱去结晶水,并生成草酸亚铁(
)固体;温度
时,草酸亚铁完全分解,发生反应:
.
(1)根据化学方程式计算草酸亚铁晶体完全脱去结晶水生成
的质量.
(2)求该草酸亚铁晶体中结晶水的质量.
(3)求该草酸亚铁晶体中铁元素的质量分数(精确到0.1%).
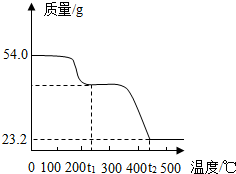
已知有些晶体按比例含有一定量特殊的水(称为结晶水),在一定的温度下可脱去结晶水,为了研究草酸亚铁晶体的组成,称取54.0g草酸亚铁晶体在隔绝空气条件下加热,得到剩余固体的质量随温度变化曲线如图所示.已知:温度
时,草酸亚铁晶体完全脱去结晶水,并生成草酸亚铁(
)固体;温度
时,草酸亚铁完全分解,发生反应:
.
(1)根据化学方程式计算草酸亚铁晶体完全脱去结晶水生成
的质量.
(2)求该草酸亚铁晶体中结晶水的质量.
(3)求该草酸亚铁晶体中铁元素的质量分数(精确到0.1%).
