水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康
(1)含有较多______________的水称为硬水,硬水加热后产生沉淀的离子方程式为__________________________( 写出生成一种沉淀物的即可) 。
(2)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:
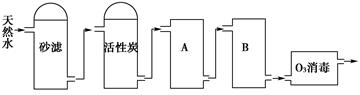
①活性炭的作用是__________________;O3消毒的优点是________________。
②A、B中放置的物质名称分别是:A__________________;B_______________。A、B中放置的物质是否可以互换?请说明原因________________________________________。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留, 从而获得纯净水的方法称为。电渗析法净化水时, 使离子通过半透膜的推动力是。
(4)检验蒸馏水的纯度时, 最简单易行的方法是测定水的 。
(5)某 城 市 用 水 中c(Ca2+)为1.0×10-3mol/L, c(Mg2+)为5.0×10-4mol/L,c(HCO3_)为8.0×10-4mol/L。如用药剂软化该1000L ,应加入Ca(OH) 2g , Na2CO 3 __________ g 。