硫酸铜是一种用途广泛的化工原料。某学习小组把适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全.通过蒸发、结晶得到硫酸铜晶体(装置如图I、Ⅱ所示)
(1)图Ⅱ是图I的改进装置。其优点有 。
(2)为符合绿色化学的要求,该学习小组进行了如下探究:将氧气直接通入到铜粉与稀硫酸的混合物中,发现常温下几乎不反应,但向混合物中加入FeSO4后再通入氧气,反应则立即发生试用离子方程式表示反应发生的原理___________________________________;在该反应中FeSO4的作用是__________________。
(3)为寻找更加适宜的氧化剂,该小组又进行了如下探究:称量3.2 g铜丝放到45 mL 1.5 mol·L-1的稀硫酸中,控温在50℃,加入18 mL 10%的H2O2,反应30 min后升温到60℃,持续反应1小时后铜丝反应完全。蒸发、冷却、结晶,过滤时用少量95%的酒精淋洗晾干,得到10 g CuSO4·5H2O。
①该实验铜丝被氧化的原理是(用离子方程式表示)_____________________________。
②反应过程中温度不宜过高的原因是________________________________________,过滤时采用酒精淋洗的优点是 。
③该小组得到硫酸铜晶体的实际产率是_____________________。
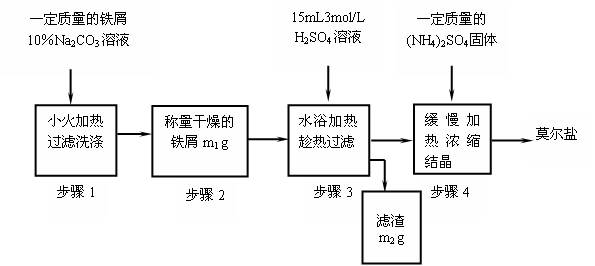
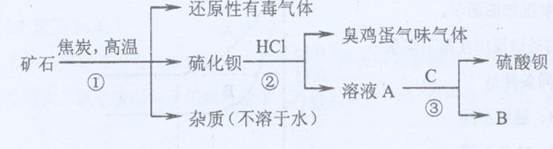 (1)写出步骤①的化学反应方程式,该反应产生的气体具有、等用途。
(1)写出步骤①的化学反应方程式,该反应产生的气体具有、等用途。
 8H20晶体和NH4Cl晶体反应过程中的能量变化⑤用蒸馏法分离两种沸点差距较大的液体⑥过滤分离互不相溶的固体和液体⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程⑧稀释浓H2SO4的过程
8H20晶体和NH4Cl晶体反应过程中的能量变化⑤用蒸馏法分离两种沸点差距较大的液体⑥过滤分离互不相溶的固体和液体⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程⑧稀释浓H2SO4的过程
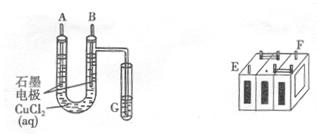
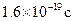 ):
):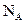 =
=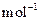
 粤公网安备 44130202000953号
粤公网安备 44130202000953号