下面两套实验装置,都涉及金属的腐蚀反应,假设其中的金属块和金属丝都是足量的。请同学们仔细观察,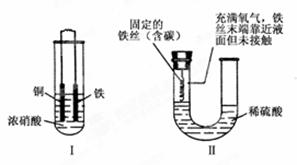
下列叙述正确的是 ( )
| A.装置Ⅰ在反应过程中自始至终只生成红棕色气体 |
| B.装置Ⅱ开始阶段铁丝只发生析氢腐蚀 |
| C.装置Ⅱ在反应过程中能产生氢气 |
| D.装置Ⅰ在反应结束时溶液中的金属阳离子只有Cu2+ |
下面两套实验装置,都涉及金属的腐蚀反应,假设其中的金属块和金属丝都是足量的。请同学们仔细观察,
下列叙述正确的是 ( )
| A.装置Ⅰ在反应过程中自始至终只生成红棕色气体 |
| B.装置Ⅱ开始阶段铁丝只发生析氢腐蚀 |
| C.装置Ⅱ在反应过程中能产生氢气 |
| D.装置Ⅰ在反应结束时溶液中的金属阳离子只有Cu2+ |