卤族元素包括F、Cl、Br、I等。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是 (填写序号)。
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷。
①下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为 ,
该功能陶瓷的化学式为 ;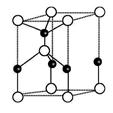
②第一电离能介于B、N之间的第二周期元素有 种。
(3)ZnCl2与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有σ键的物质的量为 。
卤族元素包括F、Cl、Br、I等。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是 (填写序号)。
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷。
①下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为 ,
该功能陶瓷的化学式为 ;
②第一电离能介于B、N之间的第二周期元素有 种。
(3)ZnCl2与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有σ键的物质的量为 。