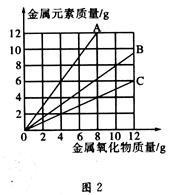
铜有两种常见的氧化物:CuO和Cu2O。某学习小组取0.98gCu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示: 
则下列分析正确的是( )
A.图1中产物A、B的化学式分别为Cu2O和CuO
B.图1整个过程中共生成0.26g水
C.图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是C
D.图1中,A到B过程中有0.01mol电子发生了转移
铜有两种常见的氧化物:CuO和Cu2O。某学习小组取0.98gCu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示: 

则下列分析正确的是( )
A.图1中产物A、B的化学式分别为Cu2O和CuO
B.图1整个过程中共生成0.26g水
C.图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是C
D.图1中,A到B过程中有0.01mol电子发生了转移