(1)铅蓄电池放电时发生下列反应负极:Pb+SO42--2e-=PbSO4 正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,用该电池电解CuSO4溶液,当有纯铜1.6g析出时,铅蓄电池内消耗硫酸物质的量为_______。
(2)锌、溴蓄电池的充、放电的电池总反应为Zn+Br2 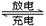 Zn2++2Br-。下列各反应①Zn-2e-====Zn2+ ②Br2+2e-====2Br- ③2Br--2e-====Br2 ④Zn2++2e-====Zn,其中充电时的阳极反应式为 ,放电时负极的反应式是 。
Zn2++2Br-。下列各反应①Zn-2e-====Zn2+ ②Br2+2e-====2Br- ③2Br--2e-====Br2 ④Zn2++2e-====Zn,其中充电时的阳极反应式为 ,放电时负极的反应式是 。
(3)目前人们正研究开发一种高能电池一—钠硫电池,它是以熔融的钠、硫为两极,以Na+导电的β,,——Al2O3陶瓷作固体电解质,反应如下:2Na+xS 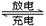 Na2Sx,其正极反应式为 ,当外电路转移4mol电子时消耗硫单质的质量为 。
Na2Sx,其正极反应式为 ,当外电路转移4mol电子时消耗硫单质的质量为 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号