一定温度下,在密闭容器内进行某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示。则下列叙述中正确的是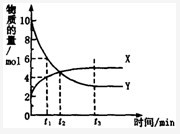
A .反应的化学方程式为2Y(g)=X(g)
B. t1时,Y的浓度是X浓度的1.5倍
C .t2时,可逆反应达到化学平衡状态
D.t3时,逆反应速率大于正反应速率
一定温度下,在密闭容器内进行某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示。则下列叙述中正确的是
A .反应的化学方程式为2Y(g)=X(g)
B. t1时,Y的浓度是X浓度的1.5倍
C .t2时,可逆反应达到化学平衡状态
D.t3时,逆反应速率大于正反应速率