(1)已知1.0mol·L—1NaHSO3溶液的pH为3.5,则此溶液离子浓度从大到小的顺序为
(用离子符号表示)。
(2)能证明Na2SO3溶液中存在水解平衡SO32-+H2O HSO3-+OH-的事实是 (填序号)。
HSO3-+OH-的事实是 (填序号)。
A.滴入酚酞溶液变红,再加入H2SO4溶液红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,在加入BaCl2溶液后产生沉淀且红色退去
(3)工业上利用催化氧化反应将SO2转化为SO3:2SO2+ O2 2SO3。若某温度下,此反应的起始浓度c(SO2)=1.0mol·L—1,c(O2)=1.5mol·L—1,达到平衡后,SO2的转化率为50%,则此温度下该反应的平衡常数K= 。
2SO3。若某温度下,此反应的起始浓度c(SO2)=1.0mol·L—1,c(O2)=1.5mol·L—1,达到平衡后,SO2的转化率为50%,则此温度下该反应的平衡常数K= 。
(4)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3-+5SO32-+2H+=I2+5SO42-+H2O。生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间衡量该反应的速率。某同学设计实验如下表所示:
| |
0.01mol/LKIO3酸性溶液(含淀粉)的体积/mL |
0.01mol·L-1 Na2SO3溶液的体积/mL |
H2O的体积/mL |
实验温度 /℃ |
溶液出现蓝色时所需时间/s |
| 实验1 |
5 |
V1 |
35 |
25 |
|
| 实验2 |
5 |
5 |
40 |
25 |
|
| 实验3 |
5 |
5 |
V2 |
0 |
|
表中V2=___________mL,该实验的目的是______________ ______。
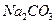 、
、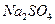 、
、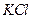 、
、 、
、 、
、 和
和 溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。
溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。
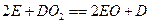 ,其中
,其中 为直线形的非极性分子。
为直线形的非极性分子。
 ⑥的单质化学方程式为___________________________。
⑥的单质化学方程式为___________________________。 溶液中由
溶液中由 电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至__________________。
电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至__________________。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号