下图中的实验装置可以用于实验室制取乙炔。请填空: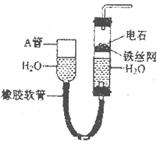
(1)图中A管的作用是______________,制取乙炔的化学反应方程式为____________________________。
(2)乙炔通入酸性KMnO4溶液中,发生___________反泣,可以观察到__________________。现象,若通入溴水中,发生______________反应。
(3)乙炔燃烧时的现象为____________________,为了安全,点燃乙炔前应先______________。
下图中的实验装置可以用于实验室制取乙炔。请填空:
(1)图中A管的作用是______________,制取乙炔的化学反应方程式为____________________________。
(2)乙炔通入酸性KMnO4溶液中,发生___________反泣,可以观察到__________________。现象,若通入溴水中,发生______________反应。
(3)乙炔燃烧时的现象为____________________,为了安全,点燃乙炔前应先______________。