现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的质量关系如下图所示。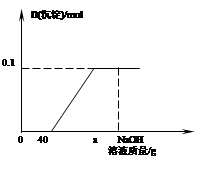
① 写出有关的反应方程式 ⒂ , ⒃ ;
② 当加入NaOH溶液质量为ag时,溶液中的溶质是 ⒄ ;
③ 求混合溶液中CuCl2的质量分数 ⒅ 。
(请根据化学方程式计算)
④ 求恰好完全反应时,消耗NaOH溶液的总质量 ⒆ 。
现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的质量关系如下图所示。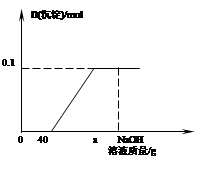
① 写出有关的反应方程式 ⒂ , ⒃ ;
② 当加入NaOH溶液质量为ag时,溶液中的溶质是 ⒄ ;
③ 求混合溶液中CuCl2的质量分数 ⒅ 。
(请根据化学方程式计算)
④ 求恰好完全反应时,消耗NaOH溶液的总质量 ⒆ 。