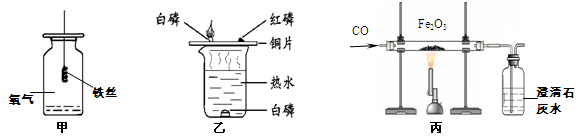
潜水艇有两种供氧的装置,第一种是储备压缩氧气,第二种是在紧急的情况下才使用的过氧化钠(Na2O2)作供氧剂,小红同学对过氧化钠如何作供氧剂产生浓厚的兴趣,于是他在老师的指导下展开了以下的探究活动。
【查阅资料】
①过氧化钠是用在矿山、坑道、潜水或宇宙飞船等缺氧的场合中,将人们呼出的CO2转换成O2,以供呼吸之用。
②二氧化碳与过氧化钠反应的生成物只有两种,一种是氧气,另一种是化合物。
③人呼出的气体中含有的水分也能与过氧化钠反应生成氧气。
(1)小红利用下图的BCDE装置组合和有关药品制取并收集氧气。
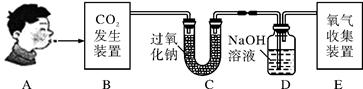
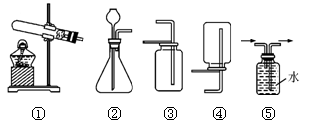
若用大理石与稀盐酸制取二氧化碳,则B中装置可采用上图中的____;E中装置可采用上图中的____ __;B中的化学方程式为: ___________________________。
(2)二氧化碳与过氧化钠反应除生成氧气外还生成什么物质?
【作出猜想】小红作出了以下三种猜想:
①生成碳酸;②生成氢氧化钠;③生成碳酸钠。
通过对反应物有关的元素组成的分析,乙同学认为猜想_______一定是错误的,理由是_________。
【进行实验】
小红通过以下实验验证了另一个猜想的正确性,请完成下述实验报告。
实验步骤
|
实验现象
|
实验结论
|
取CO2与Na2O2反应后的固体少量于试管中,加入少量__________,把产生的气体通入足量的澄清石灰水中
|
①______________;
②________________
|
猜想____是正确的
|
【反思与交流】
①小红若用图A来代替B装置,证明二氧化碳与过氧化钠反应生成了氧气,你是否同意小红的做法?____(填“是”或“否”),原因:____________________________________。
②由此可知道过氧化钠与二氧化碳反应的化学方程式为:___