某二元酸(H2A)在水中的电离方程式为:H2A = H+ + HA- HA- H+ + A2- (Ka=1.0×10-2),下列说法正确的是
H+ + A2- (Ka=1.0×10-2),下列说法正确的是
A.在0.1 mol·L-1的H2A溶液中,c(H+)> 0.12 mol·L-1
B.在0.1 mol·L-1的Na2A溶液中,c(A2-)+ c(HA-)+ c(Na+)=" 0.2" mol·L-1
C.分别将同浓度(0.1 mol·L-1)的NaHA和Na2A溶液等体积混合,其pH一定小于7
D.0.1 mol·L-1的NaHA溶液中离子浓度为:c(Na+)>c(H+)>c(HA-)>c(A2-)>c(OH-)
 2NO2(g)在下列过程中发生的变化描述正确的是()
2NO2(g)在下列过程中发生的变化描述正确的是()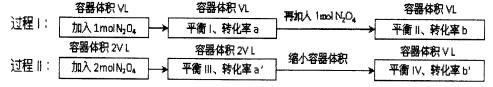
 I向平衡II过渡的过程中,v(逆)>v(正)
I向平衡II过渡的过程中,v(逆)>v(正)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号