在容积一定的密闭容器中,置入一定量的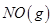 和足量
和足量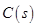 ,发生反应
,发生反应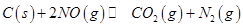 ,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是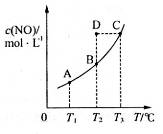
| A.该反应的△H>0 |
B.若该反应在 时的平衡常数分别为 时的平衡常数分别为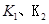 ,则 ,则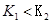 |
C.在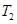 时,若反应体系处于状态D,则这时一定有 时,若反应体系处于状态D,则这时一定有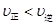 |
D.在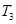 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 |
在容积一定的密闭容器中,置入一定量的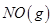 和足量
和足量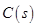 ,发生反应
,发生反应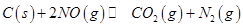 ,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
| A.该反应的△H>0 |
B.若该反应在 时的平衡常数分别为 时的平衡常数分别为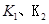 ,则 ,则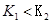 |
C.在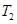 时,若反应体系处于状态D,则这时一定有 时,若反应体系处于状态D,则这时一定有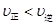 |
D.在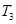 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 |