含扑热息痛高分子药物F具有长效性、稳定性,毒副作用小,而且可以实现药物的缓控释。F的一种合成流程图如下图所示: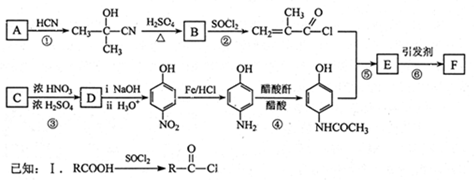
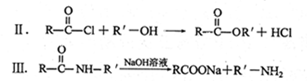
请回答下列问题:
(1)①是加成反应,则A的结构简式为_______,B中官能团的名称是________。
(2)C的名称是____________。反应②~⑥中,属于取代反应的是_________。
(3)反应⑤的化学方程式是__________________________。
(4)F与足量NaOH溶液发生反应的化学方程式是__________________________。
含扑热息痛高分子药物F具有长效性、稳定性,毒副作用小,而且可以实现药物的缓控释。F的一种合成流程图如下图所示:

请回答下列问题:
(1)①是加成反应,则A的结构简式为_______,B中官能团的名称是________。
(2)C的名称是____________。反应②~⑥中,属于取代反应的是_________。
(3)反应⑤的化学方程式是__________________________。
(4)F与足量NaOH溶液发生反应的化学方程式是__________________________。