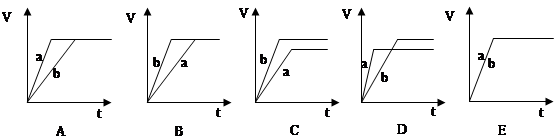按要求回答下列问题
(1)把锌片投入到盛有盐酸的敞口容器中,产生H2的速率可由图⑴表示。
在下列因素中对产生H2速率有影响的是 
①盐酸的浓度 ②锌片的表面积 ③溶液的温度 ④Cl-的浓度
| A.①④ | B.③④ | C.①②③ | D.②③ |
(2)若向等量的两份稀硫酸a和b中, 分别加入过量的锌粉, 并向a中加入少量铜粉, 下图表示产生H2的体积(V)与时间(t)的关系正确的是 ,若向a中加入少量CH3COONa固体,图像正确的是 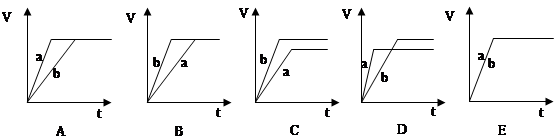
按要求回答下列问题
(1)把锌片投入到盛有盐酸的敞口容器中,产生H2的速率可由图⑴表示。
在下列因素中对产生H2速率有影响的是 
①盐酸的浓度 ②锌片的表面积 ③溶液的温度 ④Cl-的浓度
| A.①④ | B.③④ | C.①②③ | D.②③ |
(2)若向等量的两份稀硫酸a和b中, 分别加入过量的锌粉, 并向a中加入少量铜粉, 下图表示产生H2的体积(V)与时间(t)的关系正确的是 ,若向a中加入少量CH3COONa固体,图像正确的是