金属在生产生活中应用广泛。
(1)下列金属制品中,利用金属导热性的是 (填字母序号)。 
A.黄金饰品 B.铁锅 C.铜导线
(2)铁生锈的条件是 ;盐酸可用于金属表面除锈,写出盐酸除去铁锈反应的化学方程式 。
(3)某化学小组用一定量的AgNO3和Zn(NO3)2混合溶液进行了如下图所示实验。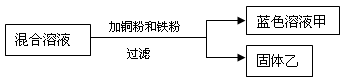
① 向乙中滴加盐酸时 (填“有”或“没有”)气泡产生。
② 甲中一定含有的溶质为 。
金属在生产生活中应用广泛。
(1)下列金属制品中,利用金属导热性的是 (填字母序号)。 
A.黄金饰品 B.铁锅 C.铜导线
(2)铁生锈的条件是 ;盐酸可用于金属表面除锈,写出盐酸除去铁锈反应的化学方程式 。
(3)某化学小组用一定量的AgNO3和Zn(NO3)2混合溶液进行了如下图所示实验。
① 向乙中滴加盐酸时 (填“有”或“没有”)气泡产生。
② 甲中一定含有的溶质为 。