I.KNO3俗名硝石,是一种重要的化工原料,在农业上用途十分广泛,下面是一种KNO3制备方法的主要步骤: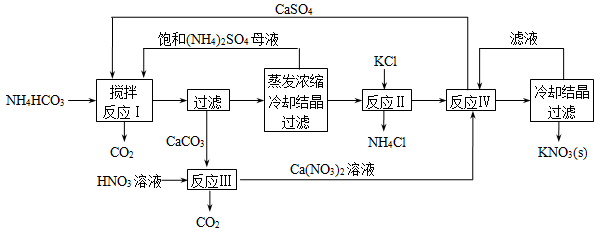
(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1︰2,该反应的化学方程式为 。
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是 ;从反应Ⅳ所得混合物中分离出CaSO4的方法是 (填“趁热过滤”、“冷却过滤”)。
(3)检验反应Ⅱ所得K2SO4中是否混有KCl的方法是:取少量K2SO4样品溶解于水, 。
(4)整个流程中,可循环利用的物质除(NH4)2SO4外,还有 (填化学式)。
(5)将硝酸与浓KCl溶液混合,也可得到KNO3,同时生成等体积的气体A和气体B。B是三原子分子,B与O2反应生成1体积黄绿色气体A和2体积红棕色气体C。B的分子式为 。
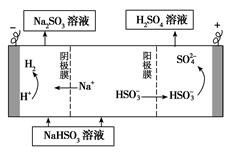
II.(1)工业上可采用电化学的方法获得N2H4,装置如右图所示,则通入氧气的 一极为 (填“正极”、“负极”),NH3反应的电极反应式为 。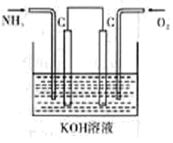
(2)肼(N2H4)可以在纯氧中燃烧生成氮气和水,为了充分利用其能量, 有人设计了原电池装置,电极材料是多孔石墨电极,电解质为能够传导H+的固体电解质,请写出负极反应式 。



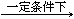 C3N6H6 +6 NH3+3CO2
C3N6H6 +6 NH3+3CO2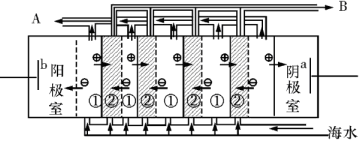
 粤公网安备 44130202000953号
粤公网安备 44130202000953号